肿瘤标志物案例13.E2假性升高案例分析
2022-07-15
1. 题目:
依西美坦致雌二醇检测结果假性升高案例分析
2.案例摘要
患者女,44岁,以“左乳癌术后13年,胸壁、锁上、对侧腋窝LNM术后(LuminalA型)”主诉于2020年4月20日就诊于本院内科门诊。患者当天复查雌二醇(E2)结果为151.9pmol/L(滤泡期:45.4-854 pmol/L;黄体期:81.9-1251 pmol/L;排卵期:151-1461 pmol/L;绝经期:18.4-505 pmol/L)。该患者双侧卵巢已切除,2019年6月开始使用依西美坦药物治疗,2019年12月CT显示左胸壁病灶较前缩小,提示治疗有效,而临床治疗有效时的预期E2水平应降低至检测下限(绝经后
3.检验科处理流程
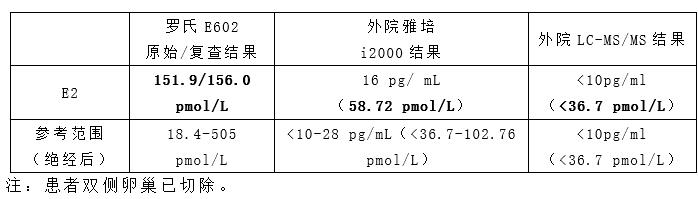
检验科确保仪器和试剂正常,室内质控在控后,将原标本进行复查,E2结果为156.0 pmol/L,与上次结果151.9 pmol/L相比,CV值为2.70%,在本实验室允许误差10%范围内。遂将结果送外单位不同的检测系统复查(本院为罗氏E602,外院为雅培I2000),结果为58.72 pmol/L(参考值:未接受激素替代疗法的绝经期

4.病史查阅
患者女,44岁,左乳癌术后13年,胸壁、锁上、对侧腋窝LNM术后(LuminalA型)。该患者于2006年8月于外院行左乳癌根治术,病理显示乳腺浸润性导管癌,ER+,PR++,Her2-。术后FAC 6程,服用他莫昔芬3年后病情稳定。2015年9月CT显示左胸壁、双锁上LN复发,行抑那通+瑞宁德化疗后E2持续下降;一年后CT复查稳定,E2降至检测下限。2017年8月行左胸壁肿物扩大切除+左腋窝淋巴结清扫术,术后PC 6程,总体疗效SD;随后来曲唑+依维莫斯治疗,期间E2水平降至检测下限附近。2019年6月左腋窝LN穿刺病理见低分化癌,ER40%+,行依西美坦+希罗达治疗;8月改用依西美坦+甲氨蝶呤+复方环磷酰胺至今。2019年12月复查CT左胸壁病灶较前稍缩小,期间E2水平215.5/177.5/125.3/191.4 pmol/L。目前疾病控制稳定。
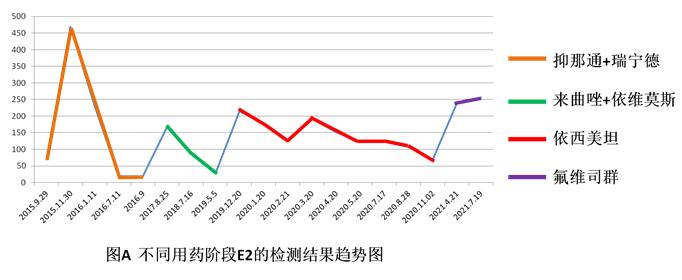
结合患者的用药史,我们发现,当患者复发时,E2水平上升;治疗有效时,E2水平下降,最低可达检测下限(见下图)。该患者依西美坦药物治疗前的来曲唑+依维莫司药物治疗有效后,E2水平下降至较低水平。而改用依西美坦+其他药物治疗,治疗有效,E2持续保持在高值水平明显与临床疗效相悖,因此临床医生在患者病情稳定时,对E2检测结果存疑是合理的。

5. 原因分析
雌激素能刺激乳腺癌细胞的生长,女性绝经期后血液中雌激素(雌酮和E2)主要来源是肾上腺和卵巢中的雄激素(雄烯二酮和睾酮)经芳香酶转化而来。通过抑制芳香酶来阻止雌激素生成是一种有效的选择性治疗绝经后激素依赖性乳腺癌的方法。绝经后激素受体阳性乳腺癌的治疗方法首选内分泌治疗[2],一线内分泌治疗首选第3代芳香化酶抑制药(AI)来曲唑,依西美坦等。AI治疗乳腺癌的有效性主要取决于E2抑制的程度。AI治疗有效后,E2水平预计会降至较低水平,LC-MS/MS法检测通常低于36.7 pmol/L [1];反之,则提示治疗失败,可考虑更换治疗药物,比如美国NCCN指南推荐的氟维司琼[3]。因此监测雌激素水平对绝经后激素受体阳性乳腺癌的临床决策具有重意义[4]。查阅资料发现,国内外均有使用特定检测方法时E2假性升高的报道[5-8],其中包括乳腺癌患者接受依西美坦治疗[8]。
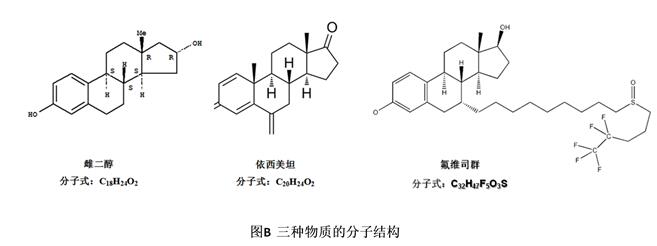
目前我科E2项目的检测方法为基于抗原抗体反应原理的电化学发光法。抗原表位(或决定簇)和抗体分子的超变区之间空间结构的互补性决定了反应的特异性。但是如果两种(或多种)来源不同的抗原拥有相同的抗原的表位(或决定簇),便可以和同一抗体发生反应,即发生交叉反应。交叉反应常发生于小分子的激素类物质的检测。E2和依西美坦分子结构非常相似(见图B),二者均由芳香环为结构特征。我们推测,在检测过程中依西美坦与检测抗体反生交叉反应,造成E2假性升高。后续在对案例患者的随访中,我们发现,患者使用和E2结构相似的另一种药物氟维司琼治疗后,血清中E2也保持在较高水平(见图A)。此前,罗氏公司于2016年发布全球安全公告,指出氟维司琼与E2检测的交叉反应,建议对接受氟维司琼治疗的患者应当采用与氟维司琼无交叉反应的检测方法(如LC-MS/MS)复测E2浓度,以准确评估绝经后患者的激素情况。本案例最终采用LC-MS/MS法,成功测得E2的真实水平,证明依西美坦也存在与E2检测抗体的交叉反应。

LC-MS/MS基本原理是样本中的成分发生电离后生成不同荷质比的离子,根据不同的质荷比,对样本进行定性和定量。质谱法只与样本的分子相关,和结构无关,不存在交叉反应,是小分子激素检测的金标准[9]。LC-MS/MS技术虽然具有无可比拟的优越性,但其价格昂贵,已开发成熟应用于临床的检测项目不多,需要专业人员进行检测,目前尚无法实现自动化和高通量标本的检测。期待在不久的将来,质谱仪应用于临床常规检测激素类小分子微量物质,满足临床需求。
至此,该患者经依西美坦治疗后血清E2持续高水平的原因已经查明,即依西美坦存在与E2检测抗体的交叉反应。同时我们积极与临床进行沟通,并将质谱法检测结果以及免疫方法检测结果告知临床,并进行了原因分析。检验和临床,对疑难检验案例的沟通和解决,真正起到了相互学习、促进、理解的作用,临床医生对此次案例分析结果非常满意。
6.专家点评
本案例表明,依西美坦能与E2检测抗体发生不同程度的交叉反应。依西美坦是临床常用的有效治疗乳腺癌患者的药物,当常规测定的E2水平与临床疗效不一致时,临床医生应考虑到E2假性升高的可能,排查治疗药物的分子结构。对于检验科,应该保证实验室的全程质量控制,积极响应来自临床的质疑。对于临床怀疑的E2结果,首先应使用不同检测系统的仪器进行复检。如果不同检测系统的仪器复检E2仍是高值,可以考虑通过LC-MS/MS质谱法对接受依西美坦治疗的患者进行E2检测,最终得到正确的E2结果。
参考文献:
[1].Owen LJ, Wu FC and Keevil BG. A rapid direct assay for the routine measurement of oestradiol and oestrone by liquid chromatography tandem mass spectrometry. Ann Clin Biochem 2014; 51(Pt 3): 360–367.
[2].Cardoso, F., et al., ESO-ESMO 2nd international consensus guidelines for advanced breast cancer (ABC2). Breast, 2014. 23(5): p. 489-502.
[3]. NCCN Clinical practice guidelines in Oncology (NCCN Guidelines) breast cancer, version 3.
[4].中国临床肿瘤学会指南工作委员会.中国临床肿瘤学会乳腺癌诊疗指南(2017.V1)[M].北京:人民卫生出版社,2017:7-8.
[5]. 翟可可,蔡莉,陈雪松,孟庆威. 氟维司琼可导致血清雌二醇检测的假阳性[J]. 临床与病理杂志, 2016, 36(6):752-755.
[6]. 李淑颖,王林杰,陈适,陈歆琦,王曦,聂敏,伍学焱,茅江峰. 检测干扰致血清雌二醇浓度假性升高2例报道及文献复习[J]. 生殖医学杂志, 2018, 28(6):588-592.
[7]. 许麾,杨洁,江泽飞. 氟维司琼致绝经后乳腺癌血清雌二醇升高1例[J]. 人民军医,2018,61(10):960-962.
[8]. Mandic, S., et al., Falsely elevated serum oestradiol due to exemestane therapy. Ann Clin Biochem, 2017. 54(3): p. 402-405.
[9]. McDonald J G,Matthew S,Auchus R J. Steroid Profiling by Gas Chromatography–Mass Spectrometry and High Performance Liquid Chromatography–Mass Spectrometry for Adrenal Diseases. Horm Cancer,2011,2(6) : 324-332.
作 者: 李小辉 中山大学肿瘤防治中心 检验科
点评专家: 戴淑琴 中山大学肿瘤防治中心 检验科






