肿瘤标志物案例1.鼻咽癌综合治疗后甲状腺功能障碍1例
前言
免疫检查点抑制剂药物开启了肿瘤治疗的新时代,改善了许多患者的预后,其作用机制在于阻断PD-L1与PD-1的结合,重新激活T细胞,以恢复T细胞的肿瘤杀伤作用。然而,由于T细胞被激活,不仅会攻击体内的癌细胞,也会损伤正常的组织细胞。因此,随着免疫检查点抑制剂的广泛应用也带来许多不良反应,称之为免疫相关不良反应(irAEs)。irAE的发生有的比较轻,有的可能导致治疗的中断,有的甚至可能危及生命,因此,irAEs的早期诊断及适当管理对治疗至关重要。
案例经过
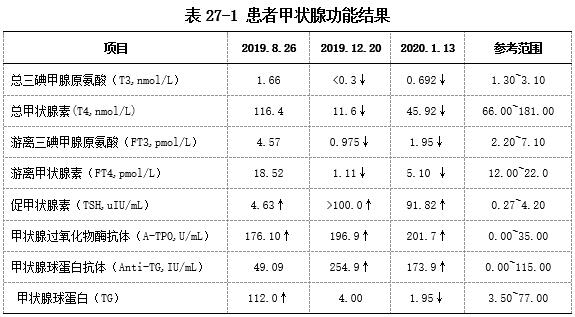
患者男, 60岁,因“鼻咽癌综合治疗后左腮腺淋巴结复发”入院治疗。患者的甲状腺功能结果异常,见表1(2019年12月20日):此类结果在肿瘤医院也不少见,许多甲状腺癌和碘治疗的患者,由于甲状腺全切和131碘治疗,患者均有发生甲状腺功能减退的可能,然而通过开单科室(非头颈科和核医学科)和诊断(鼻咽癌)可迅速排除了以上情况可能。查看患者的历史记录,患者上一次甲状腺功能检测结果(2019年8月26日)有亚甲状腺功能减退的情况,见表1。其他结果:血常规,生化检查结果无明显异常,标本状态良好。
案例分析
实验室仪器状态正常,质控在控,标本无异常情况,血常规的平均红细胞体积(MCV)与之前检查结果接近,再加上患者从6月开始就有亚甲状腺功能减退的情况,可以基本排除抽错血的可能。
那么导致患者甲状腺功能减退的原因是什么?患者的诊断为“鼻咽癌综合治疗后左腮腺淋巴结复发”,其常规的治疗方式是手术切除和/或放射治疗转移的淋巴结,这两种治疗方式均有可能对甲状腺造成损伤。查看病历:患者2016年2月于本院确诊为鼻咽癌T3N3M0IV期,行4程TP+同步放化疗,2017年2月4日结束放疗,定期随访。随后,患者因复发转移分别于2018年3月26日行“左腮腺浅叶切除术+面神经解剖术+左颈择区淋巴结清扫术”;2018年8月17日行左颈择区淋巴结清扫术;并由于再次复发于2019年8月开始对左侧腮腺病灶进行放疗,并于2019年10月22日结束放疗。
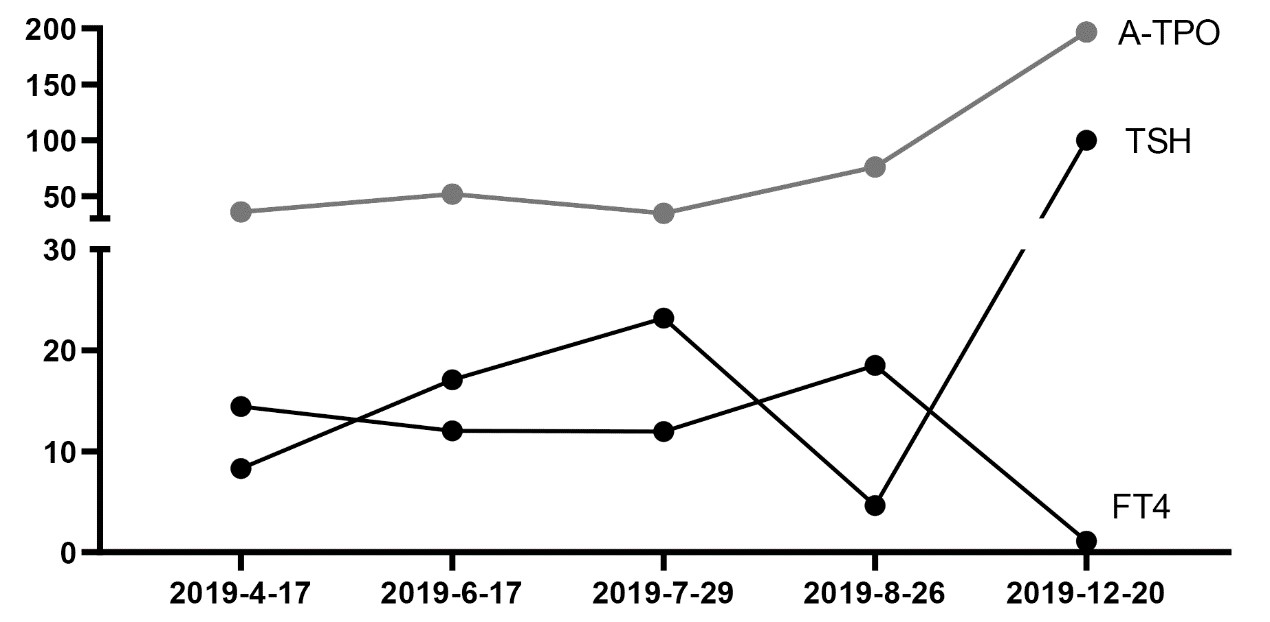
由于时间上距离较远,手术的影响基本可以排除。那么会不会是放疗导致的放射性的垂体损伤/甲状腺损伤?从时间上推测是有可能的,继续翻查检验记录。发现患者2019年8月放疗前就有亚甲状腺功能减退逐渐加重的情况(图1),因此,放射性损伤虽不能排除可能是甲状腺功能减退加重的因素之一,但却不是导致持续甲状腺功能减退的根本因素。
继续往下查看病历发现:患者于2019年3月29开始第一程Gem+DDP+pd1治疗,并完成4个疗程GP-PD1单抗治疗,但患者对化疗药物耐受性较差,停化疗,随后继续两个疗程PD-1单抗(特瑞普利单抗-拓益)治疗(2019年8月7日行第一次PD-1单抗治疗)。
使用免疫检查点抑制剂后会不同程度地出现皮疹、间质性肺炎、肠炎、肝炎、甲状腺炎等各种irAEs。甲状腺功能不全是最常见的irAE之一[1],PD-1/PD-L1阻断治疗的患者发病率高达10%。irAEs出现时间一般来说不尽相同,皮肤毒性通常用药后2~3周开始出现,胃肠道毒性通常用药后5周左右出现,肝脏和内分泌毒性通常用药后6~7周出现。该患者2019年3月29日开始Gem+DDP+pd1治疗,4月17日检测首次出现了TSH的升高,随后一路飙升,与PD1治疗内分泌不良反应的时间相符,怀疑该患者甲状腺功能“突变”是由于PD1治疗引起的。电话与医生沟通,患者现有声嘶、下巴水肿等症状,食欲尚可,患者情况基本与检验结果相符合。但患者于2019年7月26日咨询中山三院内分泌科,鉴于TSH高于10 UIu/mL,给予,左甲状腺素钠片(优甲乐)1/2片治疗。临床医生疑惑患者服用左甲状腺素钠片,甲状腺功能减退却越来越严重,因此又给患者加做了血浆皮质醇检测,结果正常(375.3 nmol/L)。医生询问是否存在其他干扰?检验科是否还有其他检测项目能辅助判断?
鉴别诊断
由于肿瘤患者的特殊性,本病例需对正常甲状腺功能病态综合征(ESS)与药物导致的中枢性甲状腺功能减退及原发性甲状腺功能减退进行鉴别。ESS又称低T3综合征,或者称为非甲状腺疾病综合征,是指一些严重的急性和慢性的全身性疾病导致甲状腺激素代谢紊乱的非甲状腺性疾病。ESS与中枢性甲状腺功能减退及原发性甲状腺功能减退区别:(1)临床表现,无论是中枢性甲状腺功能减退,还是原发性甲状腺功能减退,都有较明显的甲状腺功能减退表现和体征,但ESS的甲状腺功能减退症状一般并不明显。(2)在通常情况下,反三碘甲状腺原氨酸(rT3)水平与TT3、TT4的变化平行,在原发性甲状腺功能减退和中枢性甲状腺功能减退时,rT3同T3、T4一样表现为下降。但在重度营养不良和各种急慢性疾病伴发ESS时,会出现“分离现象”,即rT3可明显升高,而血清T3明显降低。血中促甲状腺激素、促肾上腺皮质激素和(或)卵泡刺激素/黄体生成素同时降低,提示中枢性甲状腺功能减退;而TSH升高一般提示原发性亚临床甲状腺功能减退或者甲状腺功能减退。
该患者虽未检测rT3水平,无法判断与TT3、TT4是否平行变化,但甲状腺功能减退症状明显基本可以排除ESS。患者TSH升高,血浆皮质醇正常,排除中枢性甲状腺功能减退,可以确认是原发性甲状腺功能减退,至此该报告审核发出(但是对患者服用左甲状腺素钠片甲状腺功能减退却逐渐加重还耿耿于怀)。几天后医生门诊给出答案,患者根据主观感觉间断性服用左甲状腺素钠片。2019-12-25甲状腺功能八项显示明显甲状腺功能减退时,患者已自行停止服用左甲状腺素钠片两个月。患者口服左甲状腺素钠片后自觉心率快,胃部不适,仅能耐受左甲状腺素钠片12.5 ugqd,医生强烈建议患者规律口服左甲状腺素钠片,重新规律服用两周后复查TSH开始下降,(见表12020年1月13日检测结果)。这也从另一方面验证对本病例为“免疫抑制剂造成的原发性甲状腺功能减退”的判断是正确的。
知识拓展
(1)常见导致甲状腺不良反应的抗癌药物见表2[2]。
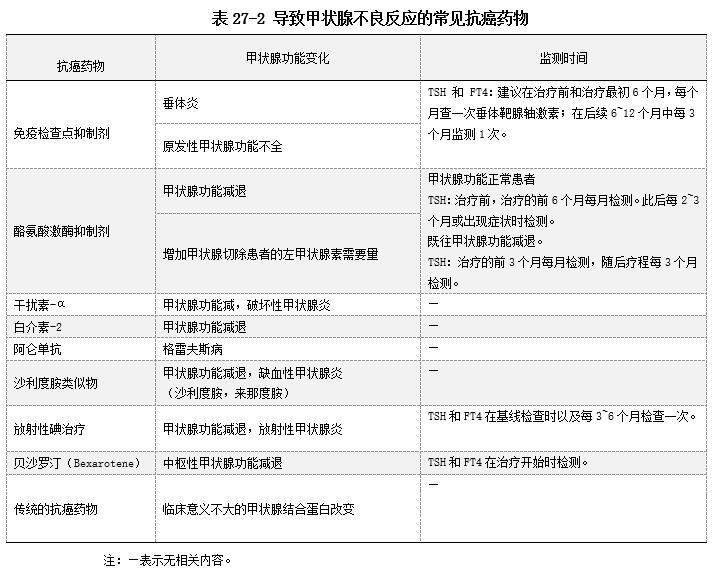
(2)免疫检查点抑制剂治疗导致的内分泌不良反应[3]:最常见的是甲状腺功能减退症、甲状腺功能亢进和垂体病。①甲状腺功能不全(10%):甲状腺功能减退症最常见,甲状腺疾病伴非特异性症状,如疲劳。由于这些症状可能比较模糊,因此,区分原发性甲状腺疾病与继发性甲状腺功能减退症对于彻底鉴别诊断至关重要。通常情况下,高TSH和T4说明原发性甲状腺功能减退症,低TSH和低游离性T4说明垂体炎。原发性甲状腺功能亢进症的发生率明显低于甲状腺功能减退症,有的患者则是先甲状腺功能亢进后甲状腺功能减退。②垂体疾病:通常垂体炎表现为疲劳和头痛的临床症状。诊断由垂体产生的低水平激素[促肾上腺皮质激素(ACTH)、TSH、促卵泡激素(FSH)、黄体生成素(LH)、生长激素(GH)、催乳素]确定。影像学上垂体腺增强和肿胀,可诊断为垂体炎。大多数患者可能因继发性甲状腺功能减退症(左旋甲状腺素治疗)或继发性肾上腺功能减退症(氢化可的松替代剂量治疗),需要长期补充受影响的激素。③肾上腺功能不全:常继发于垂体功能减退,较罕见,是最严重的不良反应,可导致脱水,低血压和电解质紊乱(高钾血症,低钠血症),易发生肾上腺危象。实验室检查结果可区分原发性肾上腺皮质功能不全(表现为低皮质醇或不当皮质醇刺激试验和高ACTH)。疑似肾上腺危象时,应该静脉注射皮质类固醇并立即住院治疗。
案例总结
药物对检验结果的干扰和影响一直是临床关注的重点和难点,在免疫检查点抑制剂治疗的过程中,内分泌激素的合理、规范监测非常重要,可以及时发现药物导致的内分泌不良反应,及时干预,可避免不必要的药物治疗中断。本案例中由于免疫抑制剂刚开始广泛应用(2019年),临床医生并未对免疫抑制剂的内分泌不良反应管理给予充分的重视,没有在PD1治疗前和治疗的前6个月对甲状腺激素进行合理、规律监测。如果能提前合理监测并及时介入,可能降低该患者的甲状腺不良反应风险,这也需要在以后的工作中进一步加强检验和临床的沟通。肿瘤患者情况比较特殊:(1)由于长期慢性或严重的消耗性疾病,机体的反应与健康人不同,诊断需排除多种原因,并充分结合病史和基线数据;(2)肿瘤患者治疗常用到糖皮质激素,过多的皮质醇可抑制垂体TSH的分泌,需要与中枢性甲状腺功能减退的结果加以鉴别;此外对于使用糖皮质激素治疗的患者需注意该类激素检测的间隔时间。
专家点评:戴淑琴(中山大学肿瘤防治中心检验科主任技师、科室副主任)
每一份报告都饱含了检验人对检验前、中、后各个环节的层层把关。本案例是药物不良反应造成的检验结果异常,是检验工作中的难点,涉及肿瘤科、检验科,特别是内分泌科等多个学科交叉,需要检验与临床互相紧密沟通。检验科不仅以提供准确可靠的检测结果为目的,将检验报告送至临床医生处后供其参考、分析;还应负责解释和咨询工作,在检测结果与患者的病情不相符,甚至对检测结果的可靠性存有些许疑虑时,更应积极深入参与临床诊疗工作,参加危重患者的诊治和病案讨论;建立多学科检验报告分析制度,发挥检验医学在全方位全周期健康服务中的重要作用。
参考文献
[1]BHATTACHARYA S,GOYAL A,KAUR P,et al.Anticancer drug-induced thyroid dysfunction[J].Eur Endocrinol,2020,16(1):32-39.
[2]BARROSO-SOUSA R,BARRY W T,GARRIDO-CASTRO A C,et al.Incidence of endocrine dysfunction following the use of different immune checkpoint inhibitor regimens: a systematic review and Meta-analysis[J].JAMA Oncol,2018,4(2):173-182.
[3]中华医学会内分泌学分会免疫内分泌学组.免疫检查点抑制剂引起的内分泌系统免疫相关不良反应专家共识(2020)[J].中华内分泌代谢杂志,2021,37(1): 1-16.






